1 概述
非妊娠及哺乳期妇女,或妇女停止授乳1年后,出现持续性溢乳且伴有闭经者,称为闭经溢乳综合征(amenorrhea galactorrhea syndrome),包括不同的病因及病理。应注意的是,闭经-溢乳综合征常常是垂体泌乳素腺瘤的症状,并在X线照片上证实肿瘤之前10年即可有此症状。闭经-溢乳综合征伴高泌乳素血症者为79%~97%。
泌乳素由腺垂体的泌乳素细胞分泌,夜间分泌增多,醒后1h逐渐降低;下丘脑合成PIF(多巴胺)及PRF(TRH)经垂体门脉到达腺垂体,调节其合成与释放泌乳素,但以PIF的作用为主,即经常处于抑制状态。5羟色胺及雌激素使垂体的泌乳细胞合成泌乳素。成年妇女血中浓度保持在20μg/L以下。正常水平的泌乳素对卵巢功能的作用尚不十分清楚,但水平过高,则阻碍卵巢黄体合成孕激素,如同时伴有LH及FSH分泌障碍,则引起不排卵而闭经。
7 流行病学
Fiedeleff等对一组围青春发育期PRL瘤(40例,女29例,男11例)的病情演变进行了仔细观察。女性患者发病年龄为8~16岁,绝大多数为微小PRL瘤。临床表现以月经紊乱、溢乳等为主。男性的发病年龄为8~17岁,绝大多数为大的PRL腺瘤,临床表现以肿瘤本身引起局部症状为突出。因此,围青春期前女性的PRL瘤与生育期患病者的表现不尽相同,药物治疗可使多数病人的促性腺激素分泌正常。
Kleinberg等分析235例(5.5%为男性)溢乳患者的临床资料,女性伴闭经者有34%存在垂体肿瘤,其血清PRL也较高,约1/3病人仅有溢乳而无闭经,在这些病人中,86%的血PRL正常,5例伴空泡蝶鞍综合征。有些人经药物、手术甚至放射治疗后仍有溢乳和(或)闭经。溴隐亭或甲磺酸麦角腈(lergotrile mesylate)可使半数病例的溢乳停止,使70%患者恢复月经。
8 病因
引起高泌乳素血症的病因很多,但高泌乳素血症不一定导致溢乳,溢乳亦非必然伴有高泌乳素血症。
8.1 生理因素
睡眠时血浆泌乳泌乳素升高,PRL分泌增多开始于睡眠后,并持续于整个睡眠过程。妊娠时PRL的分泌也增加,较非妊娠期升高10倍以上。吸吮可使PRL的分泌暂时增多,但在哺乳3个月后,上升的幅度逐渐下降。长期哺乳时,正常范围的泌乳素水平即可引起乳汁分泌;体力活动、应激、精神刺激及刺激乳头,月经黄体期均可增加泌乳素的分泌。
8.2 病理因素
(1)肿瘤性高泌乳素血症(Forbes-Albright syndrome):系下丘脑-垂体系统肿瘤所引起。据报道,该型高PRL血症占高泌乳素血症全部患者的71.6%,其中泌乳素瘤占闭经-溢乳综合-溢乳综合征的33%~76.9%。多数为微腺瘤(直径<1cm,66%),少数为巨腺瘤,占30%。肿瘤细胞不受下丘脑PIF的抑制,自主性分泌大量泌乳素。生长激素(GH)瘤、GH/PRL混合瘤、ACIH瘤及嫌色细胞瘤也可引起高泌乳素血症。肿瘤增大压迫垂体柄、腺垂体的LH及FSH分泌细胞或下丘脑的PIF及GnRH运送受阻时,则泌乳素升高伴有LH及FSH的分泌异常,发生闭经-溢乳综合-溢乳综合征。胃肠类癌或胃泌素瘤偶尔合并高GH血症和高PRL血症,病人有闭经-溢乳表现,垂体可扩大,有垂体瘤的影像学表现,切除胃肠类癌后,垂体瘤亦消退,其原因未明。垂体的促性腺激素(LH/FSH)分泌性肿瘤少见,男性患者的平均发病年龄在50岁以上,血FSH升高;女性病人的血FSH/LH亦升高,但由于绝经等原因,常不易想到本病可能,测定血清α-亚基水平可有助于早期诊断,高分辨MRI可明确诊断。当绝经后妇女出现溢乳(已绝经),血PRL升高时,要想到垂体促性腺激素分泌性肿瘤可能。如病人对多巴胺能神经激动剂治疗的反应差,疗效不明显,垂体瘤无缩小,症状无改善,或者在治疗过程中血PRL虽下降,但出现皮质醇和ACTH升高,应想到垂体泌乳素瘤衍化为ACTH瘤可能,极少数PRL瘤病人可发展为Cushing综合征(并非PRL/ACTH混合混合瘤、肿瘤细胞的PRL免疫组化染色阴性而ACTH染色阳性)。当垂体柄受压迫或由于下丘脑的调节因子(如galanin)分泌障碍可出现这一现象。除PRL瘤可与GH瘤、LH/FSH瘤、TSH瘤、α-亚基瘤并存外,还可合并中枢性尿崩症。
此外,空泡蝶鞍综合征、下丘脑及其附近的肿瘤,压迫垂体使PIF降低而致泌乳素升高。颅脑创伤、垂体意外瘤、颅咽管瘤、垂体囊肿、脑膜瘤、第3脑室血肿、蛛网膜囊肿、Rathke囊肿、多发性神经根神经炎、多发性内分泌肿瘤综合征(MEN)等亦可伴有本征。
(2)产后性高泌乳素血症(Chiafi-Frommel综合征):约占全部高泌乳素血症的30%,继发于妊娠、分娩、流产或引产后者,泌乳素一旦升高后不易下降。本症的PRL仅轻度升高,症状轻微,预后较好。
(3)特发性高泌乳素血症(Ahumada-Argonzdel Castillo综合征):少见。原因不明,多为精神创伤、应激因素所致,部分是由极微小腺瘤或大分子高泌乳素引起的。
(4)其他疾病:甲状腺功能减退并高PRL血症可能由于TRH刺激PRL释放所致。此外,Addison病、慢性肾衰也可引起PRL分泌。某些肿瘤(如支气管肺癌、肾上腺癌、胚胎癌)亦可分泌异位PRL。
原发性甲减伴闭经-溢乳综合-溢乳综合征多属甲减本身的表现,但也可能是合并有垂体PRL瘤,甲状腺激素替代治疗后,伴发的高PRL血症甚至垂体PRL瘤均可消失。产后甲状腺炎(患病率约5.5%)的发病有一定的遗传背景,也与高碘摄入等环境因素有关。甲状腺组织见浆细胞/淋巴细胞浸润,早期伴甲亢,数月后出现甲减表现,并可伴有月经紊乱、闭经-溢乳及甲状腺肿。闭经-溢乳症状较轻,多数随甲减的恢复而自行缓解。
(5)医源性高泌乳素血症(iatrogenic hyperprolactinemia):某些药物可长期抑制下丘脑合成多巴胺或影响其作用而引起泌乳素分泌,停药后可自然恢复。
抗精神病药物,尤其是安定类药物可抑制中枢多巴胺神经递质的释放,引起高PRL血症和闭经-溢乳综合-溢乳综合征,长期应用甚至导致PRL瘤。一般主张加用多巴胺激动剂,但溴隐亭又可拮抗安定类药物的作用,使病人的精神症状难以控制。Melkersson等主张在使用安定剂(如氯氮平,Clozapine)同时加用司可巴比妥(Quinalbarbitone),既有利于精神症状的控制,又防止PRL的升高。
(6)反射性因素:刺激乳头、胸部手术或胸部病变可通过神经反射刺激泌乳素分泌,泌乳素呈轻至中度升高,常伴溢乳,但不一定伴有闭经。去除病因后,血泌乳素恢复正常。
在最近的病例对照研究中,持续服用避孕药未见垂体瘤生长。前瞻性研究显示激素替代疗法对由于垂体微腺瘤所致的高泌乳素血症无不良影响。
9 发病机制
9.1 抑制下丘脑-垂体功能
高泌乳素血症抑制下丘脑多巴胺(DA)的分泌,抑制GnRH的合成和释放,使E2的正反馈反应和LH诱导的排卵峰消失。
9.2 抑制卵巢功能
降低窦状卵泡FSH、LH、PRL受体数目,加速卵泡闭锁。抑制FSH介导的粒层细胞芳香化酶活性,减少雌激素分泌,致黄体功能不全。如PRL≥100μg/ml,孕酮合成完全停止。Yoshimura等在兔离体粒层细胞培养中发现,向培养基中加入PRL后,卵泡发育受阻,卵巢类固醇激素和孕酮的合成停止,卵泡内纤溶酶原活性下降,使卵泡上皮细胞及卵泡壁不能分解,即使偶有卵泡发育成熟和排卵,其卵子的卵裂和受精能力亦明显降低,说明高水平的PRL可直接抑制卵泡发育成熟和排卵,并降低卵子的质量。
9.3 对乳腺的作用
泌乳素通过其在乳腺组织上的相应受体作用而影响乳腺的乳汁分泌,促进乳腺酪蛋白和乳白蛋白的生成,高泌乳素可引起乳腺小叶增生、巨乳和溢乳。溢乳可为自主性(显性)或隐匿性(挤压乳房时出现),可为浆液性、脂性或乳汁样。近年来人们注意到PRL在乳腺癌的发生发展中起重要作用,有人认为高泌乳素血症是乳腺癌不良预后的一个可靠指标。
10 闭经溢乳综合征的临床表现
主要表现为闭经、溢乳、血泌乳素增高和不孕。绝大部分是继发性闭经(89%),但也有原发性闭经(4%)和青春发育延迟伴高泌乳素血症的报道。闭经前多有月经稀少。2/3者合并有溢乳,可双侧性或单侧性。乳房多正常或伴小叶增生。一般先发生闭经,而溢乳常被医师发现,亦有先出现溢乳,以后出现月经紊乱乃至闭经者。高泌乳素血症时,卵巢黄体功能不足,排卵稀少或不排卵而引起不孕。泌乳素轻度增高者,可为排卵性月经,但黄体期缩短,有时可有孕激素撤退性出血。一些伴高泌乳素血症的妇女不出现溢乳,可能与同时缺乏雌激素有关。也有少数溢乳妇女泌乳素水平正常。高泌乳素血症伴排卵性月经周期者可分泌大分子泌乳素(巨泌乳素)。
长期闭经者可出现雌激素缺乏,如潮红、心悸、出汗、阴道干涩、性交疼痛、性欲减退等。头痛、肢端肥大、视力下降、视野缩小及甲状腺功能减退的表现,多为PRL瘤或下丘脑垂体病变所致。泌乳素瘤绝大部分生长缓慢,很少为巨大腺瘤,部分病人的临床症状及影像学可自发改善,甚至自行消退。
高泌乳素血症病人如未经治疗,常出现肥胖,并伴有胰岛素抵抗和骨质疏松,骨质疏松症主要与雌激素不足和PRL升高本身有关。
Fiedeleff等对一组围青春发育期PRL瘤(40例,女29例,男ll例)的病情演变进行了仔细观察。女性患者发病年龄为8~16岁,绝大多数为微小PRL瘤。临床表现以月经紊乱、溢乳等为主。男性的发病年龄为8~17岁,绝大多数为大的PRL腺瘤,临床表现以肿瘤本身引起局部症状为突出。因此,围青春期前女性的PRL瘤与生育期患病者的表现不尽相同,药物治疗可使多数病人的促性腺激素分泌正常。
Kleinberg等分析235例(5.5%为男性)溢乳患者的临床资料,女性伴闭经者有34%存在垂体肿瘤,其血清PRL也较高,约1/3病人仅有溢乳而无闭经,在这些病人中,86%的血PRL正常,5例伴空泡蝶鞍综合征。有些人经药物、手术甚至放射治疗后仍有溢乳和(或)闭经。溴隐亭或甲磺酸麦角腈(lergotrile mesylate)可使半数病例的溢乳停止,使70%患者恢复月经。
12 实验室检查
12.1 垂体功能
(1)PRL:正常生育期妇女血PRL<20μg/L,有人提出PRL20~30μg/L应行影像学方面检查。PRL50~100μg/L泌乳素瘤的发生率达20%;>100μg/L泌乳素瘤发生率达50%:PRL100~300μg发生率更高;PRL>300μg/L,如无妊娠几乎全部为垂体肿瘤所致。肿瘤越大PRL越高,如直径≤5mm,PRL为171±38μg/L;5~10mm,PRL为206±29μg/L;≥10mm,PRL为485±158μg/L。巨大腺瘤出血坏死时PRL可不升高。
药物引起者,血PRL一般在80μg/L以内,停药36h后可降至正常。雌激素引起者,停药数月后PRL可明显下降。Imai等总结Chiari-Frommel综合征(3例)、Argonzdel Castillo综合征(5例)、药物所致性闭经-溢乳综合-溢乳综合征(12例)的临床特征发现:①血PRL正常的闭经溢乳综合溢乳综合征患者所占比例相当高,其中Chiari-Frommel综合征占66.7%,Argonz-del Castillo综合征占40%,药物性者占33.3%;②许多闭经-溢乳综合-溢乳综合征血PRL,正常,对TRH等的刺激反应也无过度反应,其发生机制未明;③月经紊乱和闭经的主要原因不是LH/FSH分泌减少或分泌异常所致。
由于PRL的分泌波动较大,应多次采血测定。目前临床所用PRL放免药盒仅测定小分子PRL(2500),而不能测定大分子和巨大分子(5万~10万)PRL,故某些临床症状明显而PRL正常者,不能排除所谓隐匿型高泌乳素血症(occult hyperprolactinemia),即大分子和巨大分子高泌乳素血症。如高度疑为假性升高,应同时测定血清抗PRL抗体,或作不同组分PRL的HPLC分析与定量。
(2)FSH、LH常降低,LH/FSH比值升高。
(3)GH、TSH、ACTH根据病情需要测定。
12.2 卵巢功能检查血
E2、孕酮降低,测定E2可准确判断患者的雌激素分泌状态,孕酮测定仅用于未闭经的溢乳患者,而对闭经-溢乳者无必要。对于高泌乳素血症伴多毛者睾酮可升高。
12.3 甲状腺功能检查
合并甲减时,T3、T4降低,TSH升高。
12.4 泌乳素动态试验
(1)TRH兴奋试验:TRH除刺激垂体释放TSH外,还同时刺激PRL分泌。正常妇女1次静注TRH 100~400μg,15~30minPRL较注药前升高5~10倍,TSH升高2倍。垂体瘤时不升高,或PRL水平较基值升高不到1.5倍时,有助于泌乳素瘤的诊断。试验前应停用一切对PRL分泌有干扰的药物。饮酒和吸烟对结果无明显影响,但甘草或甘草制剂(绝大部分中药处方中含有甘草)可抑制PRL的基础分泌及TRH刺激后的最大分泌量。
(2)氯丙嗪试验(Chlorpromazine test):氯丙嗪通过受体作用,阻抑去甲肾上腺上腺上腺素吸收、转化及多巴胺功能,从而促进PRL分泌。基础状态取血后空腹服氯丙嗪25~50mg,服药后60min与120min分别取血测PRL,正常妇女经氯丙嗪兴奋后,PRL峰值较基础值增加2~5倍,垂体肿瘤者不升高。
(3)甲氧氯普氯普胺(灭吐灵)试验(胃复安,Metoclopramide test):该药为多巴胺受体拮抗剂,可促进PRL合成和释放,空腹取血后注射甲氧氯普氯普胺(灭吐灵)10mg,于注药后20、30和60min分别取血测PRL,正常人注射甲氧氯普氯普胺(胃复安)后,PRL高峰出现于20~30min,PRL峰值比基础值增加7~16倍,而功能性溢乳者,PRL升高为基础值2~3倍,泌乳素瘤者升高不明显,PRL峰值至少要超过基础值的3倍,才能认为属正常,低于以上标准者,提示有泌乳素瘤可能。
(4)维拉帕米(Verapamil)兴奋试验:维拉帕米为钙通道阻滞剂,静注维拉帕米(异搏定)后,虽不能激发正常人分泌PRL但特发性高PRL血症者的血清PRL明显升高,而垂体PRL瘤者无反应。Barbaro等认为此两组病人无重叠现象,因而是鉴别特发性高PRL血症和PRL瘤的良好试验,但对基础PRL已较高,PRL的净增值可不明显,而且维拉帕米(异搏定)试验不能将假性PRL瘤(即多巴胺能神经冲动减弱)鉴别开来。
(5)泌乳素抑制试验:左旋多巴为多巴胺前体物,经脱羧酶作用生成DA而抑制PRL分泌。正常人口服500mg后2~3hPRL明显降低。垂体肿瘤者不降低。溴隐亭为多巴胺受体激动剂,可强力抑制PRL的合成和释放。正常妇女口服2.5~5.0mg后2~4hPRL降低≥50%,持续20~30h。功能性高泌乳素血症和PRL腺瘤时下降明显,而GH、ACTH下降幅度低于前者。
13 辅助检查
13.1 蝶鞍X线断层
对垂体肿瘤诊断有重要价值,但不能发现微腺瘤,正常妇女蝶鞍前后径<17mm,深径<13mm,面积<130mm2,容积<1100mm3。如出现如下影像应作CT检查:①气球样扩大(ballooning);②双鞍底或重缘(double floor);③鞍内存在高/低密度区或密度不均质;④平皿样变形;⑤鞍上骨化(hyperostosis);⑥前后床突骨质疏松或鞍内空泡样变;⑦骨质破坏(erosion)。
13.2 CT和MRI
可行颅内病灶精确定位和放射测定。
13.3 造影检查
14 诊断
14.1 病史
着重了解闭经、溢乳出现的诱因、全身疾病及引起高泌素血症相关药物史。如病人乳罩是否合适,有无乳头瘙痒,经常摩擦等刺激,有无不耐寒、嗜睡、浮肿等甲减的病史及头痛、视力改变等与下丘脑-垂体病变有关的症状,对于可能引起高泌乳素血症的药物如避孕药、抗组胺制剂、多巴胺拮抗剂应详细了解其用法、用量及与本征的关系。
14.2 体格检查
凡闭经者,不论有无溢乳症状,均需检查双侧乳腺有无溢乳(双手轻挤压乳腺),有泌乳者即可诊断为闭经-溢乳综合-溢乳综合征,注意乳腺大小、形态、有无肿块,乳头有无皱裂,溢出物的性状和量等。同时注意全身检查,有无肢端肥大、黏液性水肿等与甲状腺及下丘脑、垂体相关方面的体征,注意检查视力、视野。妇科检查需了解与性器官和第二性征有关的体征。
14.3 眼科检查
包括视力、视野、眼压、眼底检查,以确定有无颅内肿瘤压迫征象。
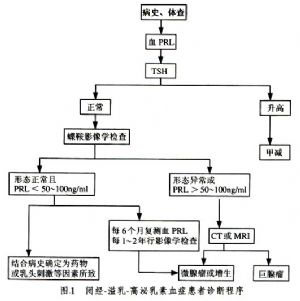
根据病史、体格检查及实验室检查发现,一般可确诊闭经-溢乳综合-溢乳综合征,并鉴别和区分引起闭经-溢乳综合-溢乳综合征的各类病因,以指导治疗(图1)。
15 鉴别诊断
1.首先询问服药史,因氯丙嗪、甲基多巴、哌嗪类、奋乃静、氟哌啶醇(氟哌丁苯)、利血平等均可引起催乳激素增多。停药后多数症状逐渐消失。除外乳腺及胸壁疾患(如手术、外伤、带状疱疹等),以及乳头刺激、长期吸吮等所引起。
2.如果在产后发病,可能是“chiari-Frommel综合征”。
3.X线蝶鞍检查提示有垂体肿瘤者,属于Forbes-Albright综合征。
4.原发甲状腺功能低下,伴有全身症状,测定甲状腺功能低下,用甲状腺激素治疗有效。
16 闭经溢乳综合征的治疗
针对病因治疗。同时用药物抑制PRL的分泌,增加PRL抑制因子活性,降低血PRL水平,达到阻止溢乳、诱发排卵、恢复月经、防止性器官萎缩等目的。
16.1 病因治疗
主要包括下列数个方面的治疗:①由药物引起者(包括口服避孕药),一般停药可自然恢复,若停药半年后月经未恢复,可用药物治疗。②原发性甲状腺功能减退者用甲状腺素制剂替代治疗,不宜因溢乳或闭经而盲目用溴隐亭治疗,如单用溴隐亭可通过下丘脑抑制TSH分泌,使病情加重。③颅内肿瘤患者,根据病情采用手术切除或放射治疗。近来临床观察,对垂体泌乳素瘤合并不孕者,单纯药物治疗优于手术及放射治疗。由于无损伤,有利于性腺轴功能的恢复,但巨腺瘤出现压迫症状时,以及溴隐亭治疗无效和无激素分泌性垂体瘤且D2受体减少者,宜手术治疗,手术前后配合溴隐亭治疗可提高疗效。
16.2 药物治疗
(1)溴隐亭:属半合成麦角碱衍生物,为多巴胺受体激动剂,促进PIF合成和分泌,抑制PRL合成和释放,并直接作用于垂体肿瘤和PRL细胞,遏制肿瘤生长和阻抑PRL、GH、TSH和ACTH分泌,适用于各种类型高泌乳素血症,也是垂体腺瘤(微腺瘤或巨腺瘤)首选疗法,尤其适合于年轻不孕患者希望生育时的治疗。一般从小剂量开始,每天1.25~2.5mg,根据血PRL、症状及基础体温变化判断疗效并调整用药剂量,当增至5mg以上,则需分次服用,70%~90%的患者治疗8周左右可恢复排卵,溢乳停止。副作用为恶心、头晕、体位性低血压等,与用量有关,停药后消失。用药期间妊娠者,不增加流产率及畸胎率,但因药物能通过胎盘并抑制胎儿PRL合成,故早期妊娠者应尽量停用溴隐亭;由于泌乳素微腺瘤的自然病程是良性的,经过几年治疗,一些病人可恢复排卵性月经。
(2)左旋多巴:在体内代谢为多巴胺,作用于下丘脑,释放PIF,每次0.2~0.5g,3次/d,可使PRL下降,促性腺激素上升,多数用药1个月后恢复月经,2个月后溢乳停止,但恶心、呕吐反应较重。
(3)八氢苯并啉(CV205-502):是一种非麦角碱类多巴胺能激动剂,为新一代特异、高效、长效的抗PRL药,适应证同溴隐亭,尤其适用于不能耐受溴隐亭、治疗无效和复发者,开始剂量0.025mg/d,睡前服用。根据治疗反应和PRL水平调整剂量,在3个月内达0.1mg/d,剂量范围为0.04~0.1mg/d。
(4)维生素B6:增加下丘脑多巴胺的转换率,从而增加PIF的作用。
多巴胺能神经激动剂为PRL瘤的主要有效治疗药物,但其疗效取决于肿瘤细胞(亦包括增生的PRL细胞和非PRL分泌性其他垂体肿瘤细胞)膜上的多巴胺D2受体的表达强度。用123Ⅰ-甲氧苯酰胺(123Ⅰ-methoxybenzamide;123I-IBZM)闪烁扫描可估计D2受体密度,如肿瘤呈123I-IBZM高摄取(D2受体高表达),一般对溴隐亭、喹高利特(Quinagolide)和卡麦角林(Cabergoline)治疗有良好反应。123I-IBZM扫描对所谓的“无功能”性垂体瘤也有重要诊断价值,尤其可筛选出适合于用多巴胺激动剂治疗的患者。
16.3 促排卵治疗
单纯溴隐亭治疗不能成功排卵和妊娠者,即采用以溴隐亭为主,配合其他促排卵药物的综合疗法,缩短治疗周期,提高排卵率和妊娠率。虽高PRL血症对排卵过程有不良影响,但不是可靠的避孕方法,事实上轻至中度(70~100ng/ml)PRL血症的患者仍能自然妊娠。另外,要求避孕的患者,避孕药能治疗高PRL血症妇女存在的低雌激素症状,研究表明激素替代治疗对垂体腺瘤所致的高泌乳素血症没有不良影响。Zennaro等报道,1例45岁妇女患闭经-溢乳综合-溢乳综合征和C型肝炎,在接受干扰素α治疗后,闭经-溢乳综合-溢乳综合征自行缓解,血PRL降至正常,干扰素α是否对PRL瘤有治疗作用,尚待进一步观察。
闭经-溢乳综合-溢乳综合征者经药物治疗后,可恢复月经、排卵及妊娠。妊娠前为微腺瘤者,妊娠后变为较大腺瘤的几率为1%,妊娠促使巨腺瘤进一步增大的几率为23%,故PRL瘤者妊娠可先停用药物治疗(至少在怀孕后4~6周内应停止药物治疗),严密观察病情变化,如发现血PRL升高与妊娠不呈比例,或见肿瘤增大,应服用多巴胺激动剂,溴隐亭对胎儿发育无明显影响,但最好选用新一代的卡麦角林(Cabergoline)。