7 概述
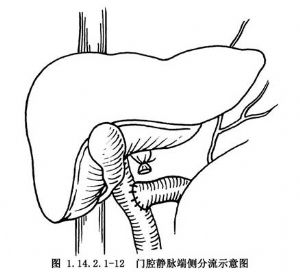
门腔静脉端-侧分流术用于门静脉高压症的手术治疗。 门腔静脉端侧分流术能直接降低门静脉压力,将门静脉入肝血流完全转流至体循环,减压作用明显,但对肝功能损害严重,肝性脑病发生率高,该术式在我国已基本不用(图1.14.2.1-1,1.14.2.1-2)。
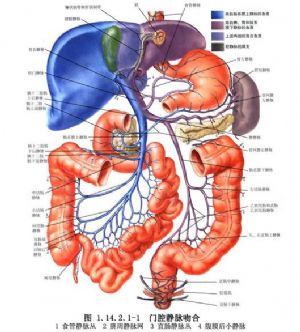

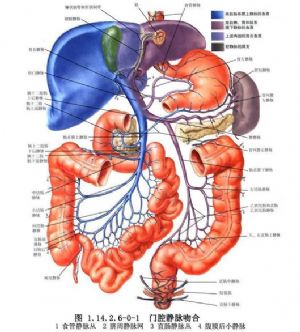
门静脉系统的两端均为毛细血管网,是一种无瓣膜的低压力静脉系统,它包括腹腔消化道内脏和肝脏两个系统。
门静脉主干由肠系膜上静脉和脾静脉于胰颈部后方汇合而成,其长度为6~8cm(图1.14.2.6-0-2)。门静脉主干形成后,经肝十二指肠韧带上行入肝分成左右干,并不断分支变小,最终于肝小叶的窦状隙以毛细血管网的形式与肝动脉毛细血管相汇合,血液流入肝小叶中央静脉,再经肝静脉入下腔静脉。
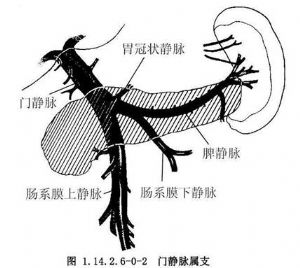
门静脉系统中,门静脉主干的解剖学变异甚少,然而,门静脉的主要属支,如肠系膜上静脉、脾静脉、胃冠状静脉的解剖学变异则不少见,并其有一定的临床意义。
8 关于门静脉高压
8.1 生理
门静脉系统和腔静脉系统之间,在肝外存在多种有着重要病理生理作用的交通支(图1.14.2.7-0-3),当门静脉压升高至一定阈值时,它们将开放形成门腔间侧支循环,分流门静脉系统血流。在门腔中,临床以胃冠状静脉(胃左静脉)、胃后静脉及胃短静脉与上腔静脉的奇静脉和半奇静脉与胃底、食管下段交通侧支最为重要。因为,在门静脉高压(protal hypertension,PHT)时,它是门体静脉间主要的交通循环通道,而由此产生的食管胃底静脉曲张及其破裂出血也是PHT所引起的最严重并发症。
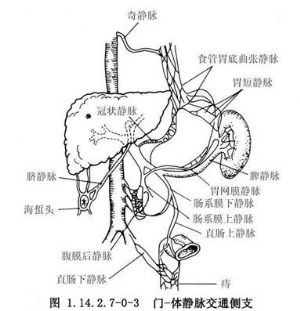
另外,在肝内窦前小叶间汇管区,肝动脉与门静脉之间亦存在许多交通支。这些动静脉交通支一般仅在肝硬变和肝内血流量增加时才开放。
门静脉主干及其属支脾静脉、肠系膜上静脉和胃冠状静脉是常用的门体分流术血管,而肠系膜上静脉作分流术的部位一般取其外科干。肠系膜上静脉外科干系指回结肠静脉与Henle干或其分支分出处间的肠系膜上静脉段。Henle干则为右结肠静脉与胃网膜右静脉汇流的静脉干。
8.2 病理
肝脏是人体内惟一有动脉和静脉双重供血的器官,其平均血流量为每分钟1500ml,几乎达心脏输出量的25%。其中,门静脉所供给的血量占肝总血流量的2/3。在门静脉血流中,约75%收集腹腔内消化器官,25%来自脾脏的血液。正常时门静脉的压力约为13~24cmH2O。若门静脉系统血液回流受阻或门静脉血流量增加,均会使门静脉压力升高。当门静脉压力超过25cmH2O,即定义为PHT;而当表现有脾脏肿大、门腔静脉间侧支循环形成以及腹水等征象时,临床上诊断为门静脉高压症。
PHT的病因很多,但在临床上约90%~95%的门静脉高压症由肝硬化所致,特别是肝炎后肝硬化为国内最常见的病因,其次是血吸虫病后肝硬化,该病在已往的流行区还不少见,而酒精性肝硬化在近年也有增多。关于PHT的分类,随着对本病研究的深入,其分类方法亦显繁杂,就手术学角度而言,分肝前、肝内及肝静脉流出道梗阻性三型即可。
肝前型PHT的常见原因为门静脉及其属支血栓形成、门静脉海绵样变,尤其是血栓形成,几乎占儿童PHT病因的50%;另外,在一些胰腺炎症或胰腺肿瘤病人中,可见单纯的脾静脉受压或血栓引发所谓的“左侧门静脉高压”(left-sided portal hypertension),或称区域性门静脉高压(regional portal hypertension)。此种PHT只有脾胃静脉的高压,而门静脉和肠系膜上静脉的压力正常,胃网膜左静脉成为主要的侧支血管,治疗上仅作脾切除就能解除PHT问题。肝静脉流出道梗阻型PHT又称布-加综合征(Budd-Chiari syndrome),多由肝静脉和(或)下腔静脉阻塞引起。
8.3 手术目的
时至今日,除肝脏移植术外,其他各种手术并不能改善肝脏原有的病变,换言之,手术只能治标不能治本。因此,无论分流术、断流术加脾切除术抑或分流术加断流术,手术目的尚限于防治食管和(或)胃底曲张静脉破裂出血以及切除巨脾治疗脾功能亢进。就此而言,一种理想的手术应能达到以下目的:①止血效果好,再出血率低;②手术对肝脏功能影响小,以免手术加重肝功能损害,引发肝功能衰竭和肝性脑病;③手术并发症少,病死率低;④术后远期效果满意,病人生存质量高。
8.4 手术适应证
(1)食管和(或)胃底曲张静脉破裂出血,经非手术治疗无法控制出血时,若病人肝脏及其他生命器官功能允许,宜不失时机地采取手术止血。
(2)食管和(或)胃底曲张静脉破裂出血,经非手术治疗控制出血后,为防再出血可行择期手术治疗。这是一种被医学界广为接受的手术适应证。因食管和(或)胃底曲张静脉一旦发生破裂出血,一年内再度出血的可能性在70%以上。
(3)食管和(或)胃底静脉重度曲张,内镜检查提示有出血倾向的病人,亦可行择期手术治疗,以防曲张静脉(首次)破裂出血的发生。有关该适应证,临床尚有一定的争议。主张手术的理由为尽管只有1/3左右的食管胃底曲张静脉并发破裂出血,但大出血的病死率很高;反对手术的观点是约2/3的食管胃底静脉曲张病人经非手术疗法可预防出血的发生,而毋需手术治疗。
(4)巨脾合并明显脾脏功能亢进和影响生活质量的PHT病人,可择期行脾切除术。若伴有中度以上食管和(或)胃底静脉曲张,也可同期加做预防出血的手术。
8.5 术式选择
(1)急诊手术:一般选择断流术。若肝功能许可,技术条件成熟,方可施行急诊分流术。对断流术后再发出血者,可行限制性的门—腔或肠—腔静脉分流术;特殊情况下,可考虑食管下端和胃近侧切除术。手术应由经验丰富的外科医师主刀实施。
(2)择期手术:原则上讲,在决定治疗方案前,应综合分析以下几方面情况:①病人条件,如全身情况、肝脏功能、凝血机制。有时,还应根据术中发现,如肝脏大小、色泽、硬度以及内脏静脉曲张情况改变术式;②所选手术对门静脉供肝血流量影响;③现时已将门静脉循环分为肠系膜和胃脾功能区,后者对食道胃底静脉曲张最有影响。因此,手术要重点针对胃脾区门静脉系统的问题;④就手术一般原则来说,在确保疗效相仿时,应选择创伤小、安全系数高,并发症少,生理功能破坏小,术后生存质量好和远期生存率高的手术;⑤还应考虑手术人员的技术问题及相关的手术设备条件等因素。
就手术原理来讲,断流术并没有影响门静脉的供肝血量,相反能维持一定的门静脉压力,增加门静脉向肝血流灌注,且手术操作较简单,易于掌握和推广应用,止血效果确切,并发症、死亡率和肝性脑病发生率均低于分流术。另外,断流术对病人条件较分流术要求要低,手术适应证较宽。因此断流术在现时国内已成为治疗PHT的主流术式。据统计,近年国内行断流术与分流术的比例为2.86∶1。断流术的主要缺点是部分文献报道的术后再出血率较高(16.3%~29.6%),究其原因是胃冠状静脉的高位食管支以及胃后静脉被遗漏,以致断流不长久所造成。此外,近年有文献报道断流术后PHG发生率高达30%。在断流术的诸多方法中,以Sugiura手术及其改良术式的断流为彻底,疗效较满意,有报道再出血率仅1.5%~3%。
门体静脉分流术对门静脉系统降压效果满意,止血率及食管静脉曲张和腹水消失率高,再出血率低,以上优点使分流术在欧美地区盛行,它也一度是国内治疗PHT出血的主要术式。但是,分流术可引发两个严重并发症:①肝功能损害加重;②分流性脑病,以致严重影响病人的生存质量,降低其远期生存率。原因是各种分流术均使肝脏的门静脉血流灌注量减少,一些门体完全分流术(如传统的门腔、脾肾、肠腔分流术等),甚至可使肝动脉的血流经门静脉逆流入下腔静脉,导致术后肝功能迅速恶化,抑或肝功能衰竭而死亡。为此,自20世纪60年代中后期及70年代初,有人开展了选择分流术和限制性分流术,其目的是在降低门静脉压力的同时,维持一定的向肝血流,取得了一定的效果;然而无论是选择性分流术还是限制性分流术,仍有14%和10%的肝性脑病发生率,以及7%和11.4%的术后再出血率,疗效不尽如人意。简而言之,门体分流术经历了近乎百年的发展,推广和改进过程几经周折起落,对其的评价尤如其他PHT手术术式,仍有许多争议,但应该说它依然是治疗PHT出血的一类重要术式。目前临床上常用的门体分流术有远端脾肾分流术、冠腔静脉分流术、限制性门腔静脉侧侧分流术、限制性门腔静脉架桥分流术,限制性肠腔静脉侧侧分流术、限制性肠腔静脉架桥分流术以及近端脾肾分流术。
分流+断流联合手术:随着对PHT研究的深入,人们已认识到治疗PHT食管胃底曲张静脉破裂出血的理想术式是在有效降低门静脉压力的同时,又能最大限度地维持门静脉向肝血流量,以免手术给肝脏功能带来进一步损害。但实际情况是单纯的断流术或分流术,因术后再出血率或术后高脑病发生率而难以达到上述手术目的。鉴此,现已不断有学者提出并偿试行分流+断流联合手术治疗PHT的临床报道,意图通过断流与分流的优势互补,以获得更好的治疗效果。目前常用的联合手术有肠腔H形架桥分流+脾切除+贲门周围血管离断术、脾肾静脉分流+脾切除+贲门周围血管离断术、TIPS+改良Sugiura手术等。但是,有关联合手术的临床实践结果尚有限,效果并非理想,而争议很多,因联合手术对病人的条件要求更高,手术创伤亦较单纯分流或断流手术更大,多数学者持反对意见,其价值或合理性尚待探讨。
8.6 手术时机
PHT病人,特别是肝炎后肝硬化患者,病情多较复杂,术后并发症多,远期预后也较差。病人术前的全身情况和肝功能状态与预后密切相关,特别是肝功能代偿的好与差,往往为手术治疗成与败的决定因素。有报道Child A、B、C级病人的手术病死率分别为2%、10%和50%左右。所以,对Child-Pugh肝功能分级属C级者,原则上不行择期手术治疗。
10 术前准备
1.给予高糖、高蛋白、高维生素、低盐和低脂肪饮食。对胃纳差的病人,应给予适当的肠外和肠内营养支持,如静脉补充GIK液和支链氨基酸,以加强营养,改善全身情况。
2.大出血后病人,若有中度以上贫血和明显的低蛋白血症,术前1周应间断输注适量新鲜全血和人体白蛋白或血浆。
3.护肝治疗 除使用一般的护肝药物外,必要时可选用肝细胞生长因子、肝细胞再生素、胰高糖素等。
4.改善凝血机制。术前1周常规肌注或静脉注射维生素K11。对凝血酶原时原时间明显延长和血小板值显著低下的病人,有条件的应于术前输注血小板悬液、冷沉淀液或新鲜冻干血浆(内含多种凝血因子的前体物质和纤维结合蛋白)。
5.预防性应用抗生素。术前30min应给予1个剂量,并备1~2个剂量术中用。抗生素应选择广谱药物,如氨基糖苷类、头孢菌素类药物;并合用抗厌氧菌药物,如甲硝唑或替硝唑。
6.消化道准备 拟作食管横断的病人,术前应予0.1%的新霉素漱口加内服,以清洗口腔和食管;术前晚宜清洁灌肠,也可用硫酸镁粉25~50g加温开水1500ml混和服用,清理肠道,以免灌肠;术前30min放置细而质软的鼻胃管,置管前宜先口服液体石蜡30ml以润滑食管。
7.术前一般应留置导尿。
12 手术步骤
1.取右肋下切口,向内可越过中线,向外至腑前线(图1.14.2.1-3)。
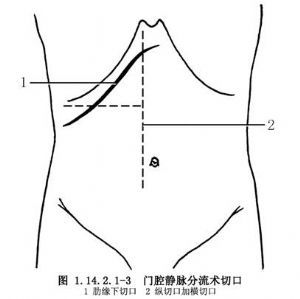
2.切开十二指肠降部侧腹膜,上至肝十二指肠韧带下方,下达降部和水平部交界处,将十二指肠向前内方翻起,显露胰头后部、胆总管下部和下腔静脉(图1.14.2.1-4)。
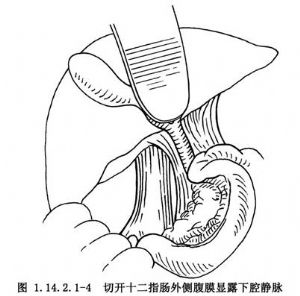
3.切开肝十二指肠韧带外侧腹膜,确认门静脉前壁和外侧壁,游离、牵拉胆总管以显示门静脉(图1.14.2.1-5)。
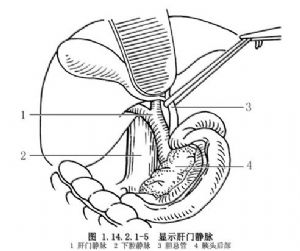
4.进一步游离门静脉后壁和内侧壁,上达门静脉分叉,下至胰头部,在胆总管和门静脉之间结扎、切断起源于门静脉主干的冠状静脉(图1.14.2.1-6)。

5.将十二指肠第二段向左前方牵拉,显示下腔静脉,切开下腔静脉前壁血管鞘,上至肝下,下达右肾静脉水平。游离下腔静脉周径2/3,长约5cm,两侧血管分支结扎后离断(图1.14.2.1-7)。

6.在十二指肠上方采用勃氏钳阻断门静脉,于门静脉左右支下方结扎切断门静脉,肝门部门静脉予以缝扎(图1.14.2.1-8)。

7.Satinsky心耳钳部分阻断下腔静脉,门静脉游离段向下腔静脉转动,在确认无张力情况下用弯形血管剪剪去下腔静脉小片前壁,形成一个较门静脉管径略大的椭圆形缺口(图1.14.2.1-9)。

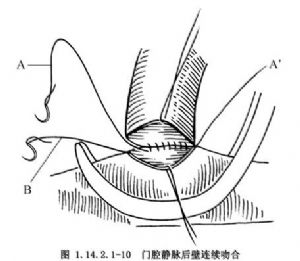
8.用5-0涤纶或聚丙烯线行门静脉和下腔静脉的端侧吻合。首先行两血管角端的缝合固定,然后采用连续外翻缝合的方法分别行吻合口后壁和前壁吻合,在关闭吻合口前壁前,开放门静脉阻断钳,排出可能存在的血凝块,再重新阻断和吻合(图1.14.2.1-10,1.14.2.1-11)。

9.先松开下腔静脉阻断钳,再开放门静脉阻断钳,若吻合口有较大裂隙,重新阻断后补缝1或2针;若出血量少,以热盐水纱布稍加压迫即可(图1.14.2.1-12)。
14 术后处理
门腔静脉端-侧分流术术后做如下处理:
1.肝炎后肝硬化门脉高门脉高压门脉高压症并发食管胃底静脉曲张出血,全身状况欠佳,肝功能有不同程度的损害,术后应加强全身支持疗法,纠正出血倾向,注意水、电解质平衡。
15 并发症
15.1 1.早期上消化道出血
门腔静脉分流术后早期上消化道出血的原因包括合并胃十二指肠溃疡、应激性溃疡、吻合口血栓形成等。术后应用洛赛克预防和治疗溃疡出血。精湛的吻合技术是预防吻合口血栓的重要步骤。术后一旦发生出血,对于肝功能已有损害的患者,极有可能发生肝功能衰竭和肝性脑病。
15.2 2.肝性脑病
门腔分流术后肝性脑病发生率高,这与分流术后氨中毒、假神经递质、氨基酸失衡等因素有关。临床可分为急性、慢性发病。一旦出现肝性脑病前驱症状,应及早治疗,除积极改善肝功能外,还应采取以下措施:①去除诱发因素;②减少过量氨的产生;③清除已产生的氨;④对抗假神经递质;⑤纠正氨基酸代谢失衡。乳果糖是预防和治疗肝性脑病的重要药物。
15.3 3.肝肾综合合征
起病急,进展快,可突然出现少尿或无尿。患者壶腹水、黄疸、神志淡漠、嗜睡,甚至昏迷。除大力护肝及防治其他并发症外,还应采用下列措施:①扩充血容量;②应用利尿剂;③应用血管活性药物;④纠正水、电解质与酸碱失衡;⑤血液透析以缓解氮质血症。